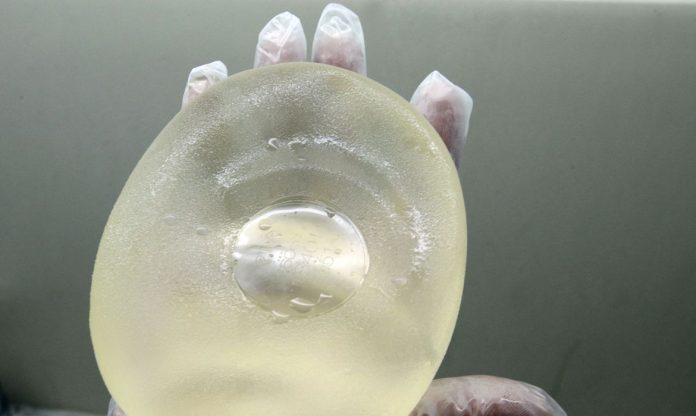
Teste de uma única amostra não atendeu especificações do órgão.
Os implantes mamários Siltex de Coesividade III e Siltex Round Gel fabricados pela empresa Mentor Medical Systems BV, situada na Holanda, com registro pela Johnson & Johnson do Brasil, tiveram suas certificações suspensas temporariamente pelo Instituto Nacional de Metrologia, Qualidade e Tecnologia (Inmetro), depois de passarem por teste mecânico de fadiga, quando uma única amostra apresentou problemas. O Inmetro informou que o órgão regulamentador dos produtos é a Agência Nacional de Vigilância Sanitária (Anvisa). Por meio da Resolução da Diretoria Colegiada (RDC) nº 16, de 21 de março de 2012, a agência estabeleceu os requisitos mínimos de identidade e qualidade para implantes mamários e exigência de certificação de conformidade do produto no âmbito do Sistema Brasileiro de Avaliação da Conformidade (SBAC).
O Inmetro informou que o órgão regulamentador dos produtos é a Agência Nacional de Vigilância Sanitária (Anvisa). Por meio da Resolução da Diretoria Colegiada (RDC) nº 16, de 21 de março de 2012, a agência estabeleceu os requisitos mínimos de identidade e qualidade para implantes mamários e exigência de certificação de conformidade do produto no âmbito do Sistema Brasileiro de Avaliação da Conformidade (SBAC).
Por meio da Portaria n.º 162, de 5 de abril de 2012, o Inmetro instituiu, no âmbito do SBAC, a certificação compulsória para implantes mamários, que deve ser realizada por Organismo de Certificação de Produto (OCP), acreditado pelo instituto. Desse modo, a certificação dos implantes mamários atestou que o produto atende aos requisitos de identidade e qualidade, definidos pela Anvisa. Cabe ainda à agência o registro do produto implante mamário, bem como as ações de fiscalização e de penalização em casos de descumprimento das disposições contidas na RDC nº 16, de 2012, segundo o Inmetro.
Nota
Em nota, a Johnson & Johnson Medical Devices no Brasil afirmou que “nada é mais importante para a Mentor do que a saúde e a segurança dos pacientes que escolhem os nossos implantes. O Inmetro suspendeu temporariamente o certificado da Mentor para a família de produtos de implantes mamários Siltex de Coesividade III e Siltex Round Gel, após o teste de uma única amostra não atender às especificações do órgão certificador.
A Mentor interrompeu a distribuição desses produtos no Brasil até que o certificado seja restabelecido. “Nossa revisão concluiu que esse episódio não está relacionado à qualidade, segurança ou eficácia do produto, e nenhuma ação é necessária para os pacientes. Estamos trabalhando em estreita colaboração com o Inmetro para resolver esse assunto”, diz a nota.
Ensaio de fadiga
A Agência Nacional de Vigilância Sanitária (Anvisa) reiterou que, de acordo com a Resolução RDC nº 16, “os implantes mamários devem atender às exigências e aos requisitos mínimos de qualidade, conforme ensaios, procedimentos e metodologias descritos na Norma Técnica ISO 14.607”. O ensaio de fadiga é um dos requisitos que deve estar em conformidade com o estabelecido nessa norma.
A finalidade do ensaio de fadiga é simular o desempenho do produto a longo prazo. “Portanto, pode indicar um comprometimento na vida útil do produto”, explicou a Anvisa, por meio de sua assessoria de imprensa. A agência informou que as duas marcas voltarão a ser comercializadas “quando atenderem a todos os requisitos estabelecidos nos regulamentos tanto da Anvisa quanto do Inmetro”.
Recomendações
A gerente-geral de Monitoramento de Produtos Sujeitos à Vigilância Sanitária da Anvisa, Suzie Marie Gomes, afirmou que, em princípio, não há razão para preocupação por parte das mulheres e homens que fizeram implantes mamários com essas duas marcas.
“Até o momento, não foram identificados riscos, ou riscos adicionais, em decorrência da suspensão temporária da certificação do produto. As complicações e efeitos indesejáveis que o paciente, porventura, possa vir a ter com o uso do produto, em princípio, estão descritos na instrução de uso”.
A mensagem é que os pacientes implantados devem seguir o acompanhamento médico de forma regular e, caso tenham algum evento adverso relacionado ao implante, devem enviar notificação pelo endereço eletrônico da Anvisa.
Segurança
Na análise do cirurgião plástico Fernando Amato, membro da Sociedade Brasileira de Cirurgia Plástica (SBCP), “a suspensão [das marcas de implantes mamários] é um protocolo de segurança, até que sejam concluídas todas as análises. Portanto, no momento, não oferece risco às pacientes que utilizam esses dois produtos”.
Amato enfatizou a importância do contato permanente da paciente com seu médico para que, em momentos como esse, ela possa receber os esclarecimentos necessários.
O especialista acrescentou que, embora seja raro, pode haver ruptura do implante mamário com o passar dos anos e, “mesmo não existindo prazo de validade, é importante um acompanhamento com o cirurgião plástico”, indicou. As trocas dos implantes podem ocorrer a cada dez anos.
*Informações/AgênciaBrasil